
Les problèmes qPCR lncRNA font partie des difficultés les plus fréquentes en analyse de l’expression génique, notamment lorsque les chercheurs travaillent sur des transcrits faiblement exprimés, peu annotés ou présents sous plusieurs isoformes.
Même si la qPCR est une technique sensible, les longs ARN non codants restent souvent difficiles à mesurer de manière fiable. Ces particularités peuvent entraîner des signaux faibles, des résultats variables, une amplification non spécifique ou une mauvaise reproductibilité entre expériences.
Pour obtenir des données exploitables, il est essentiel de comprendre l’origine de ces problèmes et d’adapter le workflow qPCR aux caractéristiques des lncRNA. Dans cet article, nous passons en revue les principales causes d’échec, les bonnes pratiques pour les corriger et les points de contrôle à intégrer pour renforcer la fiabilité de vos résultats.
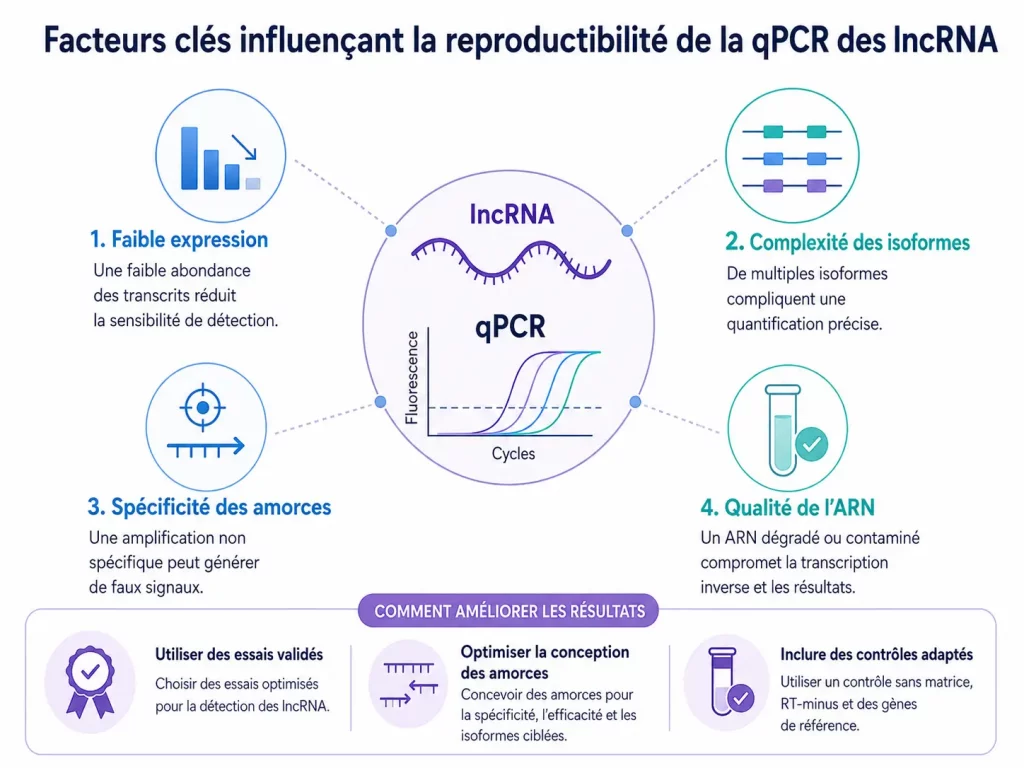
Les problèmes rencontrés lors de l’analyse des lncRNA par qPCR sont souvent liés à la nature même de ces transcrits. Contrairement à de nombreux gènes codants, les lncRNA peuvent être faiblement exprimés, spécifiques d’un tissu ou d’un état cellulaire, et parfois difficiles à distinguer d’autres transcrits proches.
Les difficultés les plus fréquentes incluent :
Ces problèmes peuvent compromettre l’interprétation des données, en particulier dans les projets de validation RNA-seq, de découverte de biomarqueurs ou d’analyse de voies biologiques.
Les lncRNA présentent plusieurs caractéristiques qui rendent leur quantification plus complexe. Beaucoup sont exprimés à de faibles niveaux, parfois proches de la limite de détection. Certains existent sous plusieurs isoformes ou se chevauchent avec des régions codantes, ce qui complique la conception d’amorces réellement spécifiques.
L’annotation des lncRNA peut également varier selon les bases de données, les versions de génomes de référence ou les méthodes de transcriptomique utilisées. Un essai qPCR mal ciblé peut donc mesurer un signal partiel, non spécifique ou difficile à relier à l’isoforme d’intérêt.
C’est pourquoi l’analyse qPCR des lncRNA demande souvent une approche plus rigoureuse que les workflows standards d’expression génique.
La faible abondance des transcrits est l’un des principaux obstacles en qPCR lncRNA. Lorsqu’un lncRNA est exprimé à très bas niveau, le signal peut être instable, difficile à distinguer du bruit de fond ou fortement influencé par de petites variations techniques.
Cela peut entraîner :
Comment améliorer la détection des lncRNA faiblement exprimés
Pour limiter ces problèmes, il est recommandé de travailler sur plusieurs points du workflow :
Pour les lncRNA très faiblement exprimés ou les échantillons limités, une stratégie de préamplification peut être utile. Des approches comme SpeAmp® peuvent aider à améliorer la sensibilité de détection, à condition d’être utilisées dans un workflow contrôlé et adapté aux objectifs expérimentaux.
La conception des amorces est un point critique en qPCR lncRNA. Une paire d’amorces mal conçue peut amplifier une cible non souhaitée, détecter plusieurs isoformes à la fois ou générer un signal qui ne reflète pas correctement le transcrit étudié.
Les principaux risques sont :
Bonnes pratiques pour améliorer la spécificité
Pour renforcer la fiabilité des résultats, il est important de :
Dans le cas des lncRNA, la spécificité n’est pas un détail technique : elle conditionne directement la valeur biologique du résultat.
De nombreux lncRNA existent sous plusieurs variants transcriptomiques. Cette diversité peut compliquer la quantification, car un essai qPCR peut mesurer une isoforme précise, plusieurs isoformes simultanément ou une région commune qui ne permet pas de distinguer les variants.
Cette complexité peut provoquer :
Avant de concevoir ou de sélectionner un essai qPCR, il est donc essentiel de clarifier l’objectif biologique : cherche-t-on à mesurer toutes les isoformes d’un lncRNA, une isoforme spécifique, ou simplement à confirmer la présence d’un signal transcriptomique observé en RNA-seq ?
Cette étape permet d’éviter de comparer des données qui ne mesurent pas exactement la même entité moléculaire.
Même avec de bonnes amorces, la qPCR lncRNA peut être perturbée par des variations expérimentales. La qualité de l’ARN, l’efficacité de la transcription inverse, la normalisation ou les différences de manipulation peuvent influencer fortement les résultats, surtout lorsque les transcrits sont peu abondants.
Les sources fréquentes de variabilité incluent :
Comment limiter la variabilité
Pour améliorer la reproductibilité, il est recommandé de :
La reproductibilité dépend rarement d’un seul paramètre. Elle repose plutôt sur l’ensemble du workflow, depuis l’extraction de l’ARN jusqu’à l’analyse des données.
Pour obtenir des résultats plus fiables en qPCR lncRNA, il faut combiner une bonne conception expérimentale, des essais validés et des contrôles adaptés.
Les actions prioritaires sont :
Ces bonnes pratiques permettent d’améliorer la sensibilité, la spécificité et la reproductibilité des analyses, en particulier pour les transcrits faiblement exprimés ou les projets de validation RNA-seq.
Pour les cibles lncRNA complexes, les approches qPCR standards ne suffisent pas toujours. Les difficultés liées à la faible expression, aux isoformes et à la spécificité des amorces peuvent rendre les résultats difficiles à interpréter.
AnyGenes® développe des solutions qPCR et qPCR arrays conçues pour accompagner l’analyse ciblée de l’expression génique, y compris pour les transcrits complexes ou faiblement abondants.
Ces solutions peuvent aider à :
L’objectif n’est pas seulement d’obtenir un signal qPCR, mais de générer une donnée interprétable, cohérente avec la question biologique et exploitable dans un contexte de recherche.
Les problèmes de qPCR lncRNA deviennent particulièrement critiques lorsque les résultats orientent des décisions scientifiques importantes. C’est souvent le cas dans les projets de :
Dans ces contextes, un signal non spécifique ou une mauvaise reproductibilité peut conduire à des conclusions erronées, à la sélection de mauvais candidats ou à une perte de temps dans les étapes de validation.
Une approche rigoureuse dès le départ permet donc de réduire le risque expérimental et d’améliorer la qualité des données générées.
Ces problèmes peuvent compromettre l’interprétation des données, en particulier dans les projets de validation RNA-seq, de découverte de biomarqueurs ou d’analyse de voies biologiques.
L’analyse des lncRNA par qPCR demande souvent plus de précaution qu’une analyse classique de gènes codants. Les faibles niveaux d’expression, la complexité des isoformes et les risques de signaux non spécifiques imposent une attention particulière à la conception des essais, aux contrôles et à la normalisation.
Pour les transcrits complexes ou peu abondants, des essais validés et des workflows optimisés sont essentiels pour obtenir des résultats spécifiques, reproductibles et biologiquement interprétables.
La qPCR des lncRNA échoue souvent en raison de faibles niveaux d’expression, d’une complexité importante des isoformes, d’une spécificité insuffisante des amorces ou d’une qualité d’ARN insuffisante. Ces facteurs peuvent entraîner des signaux faibles, variables ou non spécifiques.
Les résultats peuvent être améliorés en utilisant des essais validés, en optimisant la conception des amorces, en contrôlant la qualité de l’ARN, en choisissant des gènes de référence adaptés et en intégrant des contrôles expérimentaux appropriés.
Le principal problème est souvent la combinaison entre une faible expression des transcrits et une forte complexité transcriptomique. Cette combinaison rend la détection plus difficile et augmente le risque de variabilité ou de mauvaise interprétation.
Des amorces standards peuvent être utilisées, mais elles ne garantissent pas toujours une détection fiable des lncRNA. Pour les transcrits complexes, faiblement exprimés ou proches d’autres régions génomiques, des essais validés sont recommandés.
Les différences peuvent venir du fait que le RNA-seq et la qPCR ne ciblent pas toujours exactement la même région du transcrit ou la même isoforme. La profondeur de séquençage, l’annotation utilisée, la spécificité des amorces et le niveau d’expression peuvent également expliquer ces écarts.
Si vous rencontrez des problèmes de reproductibilité, de spécificité ou de détection sur des lncRNA, AnyGenes® peut vous accompagner dans le choix d’une approche adaptée à vos cibles et à vos échantillons. Nos solutions qPCR et qPCR arrays sont conçues pour soutenir l’analyse ciblée de l’expression génique, la détection de transcrits faiblement exprimés et la validation de résultats RNA-seq.
Contactez nos experts pour améliorer votre workflow qPCR lncRNA.
